Какое строение имеет металлическая кристаллическая решетка
1.3.3. Вещества молекулярного и немолекулярного строения. Тип кристаллической решётки. Зависимость свойств веществ от их состава и строения.
Для большинства веществ характерна способность в зависимости от условий находиться в одном из трех агрегатных состояний: твердом, жидком или газообразном.
Например, вода при нормальном давлении в интервале температур 0-100 o C является жидкостью, при температуре выше 100 о С способна существовать только в газообразном состоянии, а при температуре менее 0 о С представляет собой твердое вещество.
Вещества в твердом состоянии различают аморфные и кристаллические.
Характерными признаками аморфных веществ является отсутствие четкой температуры плавления: их текучесть плавно увеличивается с ростом температуры. К аморфным веществам относятся такие соединения, как воск, парафин, большинство пластмасс, стекло и т.д.
Все же кристаллические вещества обладают конкретной температурой плавления, т.е. вещество с кристаллическим строением переходит из твердого состоянии в жидкое не постепенно, а резко, при достижении конкретной температуры. В качестве примера кристаллических веществ можно привести поваренную соль, сахар, лед.
Разница в физических свойствах аморфных и кристаллических твердых веществ обусловлена прежде всего особенностями строения таких веществ. В чем заключается разница между веществом в аморфном и кристаллическом состоянии, проще всего понять из следующей иллюстрации:
Как можно заметить, в аморфном веществе, в отличие от кристаллического, отсутствует какой-либо порядок в расположении частиц. Если же в кристаллическом веществе мысленно соединить прямой два близкорасположенных друг к другу атома, то можно обнаружить, что на этой линии на строго определенных промежутках будут лежать одни и те же частицы:
Таким образом, в случае кристаллических веществах можно говорить о таком понятии, как кристаллическая решетка.
Кристаллической решеткой называют пространственный каркас, соединяющий точки пространства, в которых находятся частицы, образующие кристалл.
Точки пространства, в которых находятся образующие кристалл частицы, называют узлами кристаллической решетки.
В зависимости от того, какие частицы находятся в узлах кристаллической решетки, различают: молекулярную, атомную, ионную и металлическую кристаллические решетки.
В узлах молекулярной кристаллической решетки
находятся молекулы, внутри которых атомы связаны прочными ковалентными связями, однако сами молекулы удерживаются друг возле друга слабыми межмолекулярными силами. Вследствие таких слабых межмолекулярных взаимодействий кристаллы с молекулярной решеткой являются непрочными. Такие вещества от веществ с иными типами строения отличаются существенно более низкими температурами плавления и кипения, не проводят электрический ток, могут как растворяться, так и не растворяться в различных растворителях. Растворы таких соединений могут как проводить, так и не проводить электрический ток в зависимости от класса соединения. К соединениям с молекулярной кристаллической решеткой относятся многие простые вещества — неметаллы (отвержденные H2, O2, Cl2, ромбическая сера S8, белый фосфор P4), а также многие сложные вещества – водородные соединения неметаллов, кислоты, оксиды неметаллов, большинство органических веществ. Следует отметить, что, если вещество находится в газообразном или жидком состоянии, говорить о молекулярной кристаллической решетке неуместно: корректнее использовать термин — молекулярный тип строения.
Кристаллическая решетка алмаза как пример атомной решетки
В узлах атомной кристаллической решетки
находятся атомы. При этом все узлы такой кристаллической решетки «сшиты» между собой посредством прочных ковалентных связей в единый кристалл. Фактически, такой кристалл является одной гигантской молекулой. Вследствие особенностей строения все вещества с атомной кристаллической решеткой являются твердыми, обладают высокими температурами плавления, химически мало активны, не растворимы ни в воде, ни в органических растворителях, а их расплавы не проводят электрический ток. Следует запомнить, что к веществам с атомным типом строения из простых веществ относятся бор B, углерод C (алмаз и графит), кремний Si, из сложных веществ — диоксид кремния SiO2 (кварц), карбид кремния SiC, нитрид бора BN.
У веществ с ионной кристаллической решеткой
в узлах решетки находятся ионы, связанные друг с другом посредством ионных связей.
Поскольку ионные связи достаточно прочны, вещества с ионной решеткой обладают сравнительно высокой твердостью и тугоплавкостью. Чаще всего они растворимы в воде, а их растворы, как и расплавы проводят электрический ток.
К веществам с ионным типом кристаллической решетки относятся соли металлов и аммония (NH4 + ), основания, оксиды металлов. Верным признаком ионного строения вещества является наличие в его составе одновременно атомов типичного металла и неметалла.
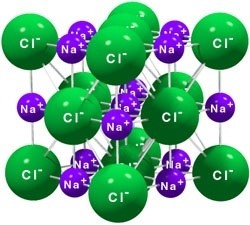 Кристаллическая решетка хлорида натрия как пример ионной решетки
Кристаллическая решетка хлорида натрия как пример ионной решетки
Однако следует отметить, что в веществах с ионным типом строения нередко можно обнаружить, помимо ионных, также ковалентные полярные связи. Это наблюдается в случае сложных ионов, т.е. состоящих из двух или более химических элементов (SO4 2- , NH4 + , PO4 3- и т.д.). Внутри таких сложных ионов атомы связаны друг с другом ковалентными связями.
Металлическая кристаллическая решетка
наблюдается в кристаллах свободных металлов, например, натрия Na, железа Fe, магния Mg и т.д. В случае металлической кристаллической решетки, в ее узлах находятся катионы и атомы металлов, между которыми движутся электроны. При этом движущиеся электроны периодически присоединяются к катионам, таким образом нейтрализуя их заряд, а отдельные нейтральные атомы металлов взамен «отпускают» часть своих электронов, превращаясь, в свою очередь, в катионы. Фактически, «свободные» электроны принадлежат не отдельным атомам, а всему кристаллу.
Металлическая кристаллическая решетка
Такие особенности строения приводят к тому, что металлы хорошо проводят тепло и электрический ток, часто обладают высокой пластичностью (ковкостью).
Разброс значений температур плавления металлов очень велик. Так, например, температура плавления ртути составляет примерно минус 39 о С (жидкая в обычных условиях), а вольфрама — 3422 °C. Следует отметить, что в обычных условиях все металлы, кроме ртути, являются твердыми веществами.
Строение металлов. Атомно-кристаллическое строение металлов.
Данные свойства обусловлены особенностями строения металлов. Согласно теории металлического состояния, металл представляет собой вещество, состоящее из положительных ядер, вокруг которых по орбиталям вращаются электроны. На последнем уровне число электронов невелико и они слабо связаны с ядром. Эти электроны имеют возможность перемещаться по всему объему металла, т.е. принадлежать целой совокупности атомов.
Таким образом, пластичность, теплопроводность и электропроводность обеспечиваются наличием «электронного газа».
Зависимость свойств веществ от их состава. Строение вещества. Типы кристаллических решеток. Ионные кристаллические решетки
Урок открытых мыслей
Цели . Образовательная – закрепить и углубить знания учащихся по теории химического строения, ее основным положениям.
Воспитательная – содействовать формированию причинно-следственных связей и отношений.
Развивающая – развитие мыслительных умений, способности переносить знания и умения в новые ситуации.
Оборудование и реактивы. Набор шаростержневых моделей; образцы натурального и синтетического каучука, диэтиловый эфир, бутанол, этанол, фенол, литий, натрий, раствор лакмуса, бромная вода, муравьиная и уксусная кислоты.
Девиз . «Всякое вещество – от самого простого до самого сложного – имеет три различные, но взаимосвязанные стороны – свойство, состав, строение» (В.М.Кедров).
ХОД УРОКА
Что включает в себя понятие «зависимость»? (Узнать мнение учащихся).
На доске написать определение: «Зависимость –
1) отношение одного явления к другому как следствие к причине;
2) подчиненность другим при отсутствии самостоятельности, свободы» (словарь С.И.Ожегова).
Цели урока определим совместно, составив схему:
Мотивационно-ориентационный блок
Определите верность приведенных ниже суждений, подтвердите ваши ответы примерами.
Теорию химического строения открыл Д.И.Менделеев.
Ответ . А.М.Бутлеров, 1861 г.
Валентность углерода в органических соединениях может быть II и IV.
Ответ . Валентность углерода – чаще всего IV.
Атомы, образующие молекулы органических веществ, связаны беспорядочно, без учета валентности.
Ответ . Атомы в молекулах связаны в определенной последовательности согласно их валентности.
Свойства веществ не зависят от строения молекул.
Ответ . Бутлеров в теории химического строения утверждал, что свойства органических соединений определяются составом и строением их молекул.
Операционно-исполнительный блок
Фактор пространственного строения
Что вам известно о пространственном строении молекул алканов и алкенов?
Ответ . В алканах при каждом углероде – четыре соседних атома, которые располагаются в вершинах тетраэдра. Сам углерод находится в центре тетраэдра. Тип гибридизации атома углерода – sp 3 , углы между связями (Н–С–С, Н–С–Н, С–С–С) — 109°28″. Строение углеродной цепи – зигзагообразное.
В алкенах два атома углерода, связанных двойной связью, и четыре атома при них с одинарными связями находятся в одной плоскости. Тип гибридизации атомов – sp 2 , углы между связями (Н–С=С, C–С=С) — 120°.
Вспомните, в чем отличие пространственного строения молекул натурального каучука и синтетического.
Ответ . Натуральный каучук – линейный полимер изопрена – имеет строение цис -1,4-полиизопрена. Синтетический каучук может иметь строение транс -1,4-полиизопрена.

Одинакова ли эластичность этих каучуков?
Ответ . Цисформа более эластична, чем трансформа. Молекулы натурального каучука длиннее и более упруго закручены (сначала в спираль, а потом в клубок), чем молекулы синтетического каучука.
Крахмал (С 5 Н 10 О 5) m – белый аморфный порошок, а целлюлоза (С 5 Н 10 О 5) n – волокнистое вещество.
В чем причина такого различия?
Ответ . Крахмал – полимер -глюкозы, тогда как целлюлоза – полимер-глюкозы.

Отличаются ли химические свойства крахмала и целлюлозы?
Ответ . Крахмал + I 2 синий р-р,
целлюлоза + HNO 3 нитроцеллюлоза.
Вывод . От пространственного строения зависят как физические, так и химические свойства.
Фактор химического строения
Что является главной идеей теории химического строения?
Ответ . Химическое строение отражает зависимость свойств веществ от порядка соединения атомов и их взаимодействия.
Определите, что общего у веществ:
Ответ . Состав.
Сравните физические свойства данных веществ. В чем вы видите причину такого отличия?
На основании распределения электронной плотности химической связи определите, какая молекула более полярна? С чем это связано?
Ответ . –ОН водородную связь.
Демонстрационный эксперимент

Вывод . Реакционная способность спирта определяется взаимным влиянием атомов в молекуле.
Фактор электронного строения
В чем заключается сущность взаимного влияния атомов?
Ответ . Взаимное влияние состоит во взаимодействии электронных структур атомов, что приводит к смещению электронной плотности химических связей.
Лабораторная работа
Учитель . На ваших столах стоят наборы для лабораторной работы. Выполните задание и докажите экспериментально зависимость свойств веществ от электронного строения. Работа в парах. Строго соблюдайте правила техники безопасности.
Вариант I . Проведите исследование химических свойств этанола и фенола. Докажите зависимость их реакционной способности от электронного строения. Используйте реагенты – металлический литий и бромную воду. Составьте уравнения возможных реакций. Покажите смещение электронной плотности химической связи в молекулах.
Вариант II . Поясните сущность взаимного влияния карбоксильной группы –СООН и заместителя при карбонильном углероде в молекулах карбоновых кислот. Рассмотрите на примере муравьиной и уксусной кислот. Используйте раствор лакмуса и литий. Составьте уравнения реакций. Покажите смещение электронной плотности химической связи в молекулах.
Вывод . Химические свойства зависят от взаимного влияния атомов.


Итоговый контроль знаний
Учитель . Подведем итог нашего урока. Мы с вами подтвердили, что свойства веществ зависят от пространственного химического и электронного строения.
1. Формулы НСООН, С 6 Н 5 ОН и C 4 H 9 COОН запишите в порядке возрастания кислотных свойств веществ.
2. Расположите формулы СН 3 СООН, С 3 Н 7 СООН, СН 3 ОН, ClCH 2 СООН в порядке убывания кислотных свойств веществ.
3. У какого альдегида:

более активная альдегидная группа? Почему?
Оцените свою работу на уроке.
Л.А.ЕРЕМИНА,
учитель химии школы № 24
(г. Абакан, Хакасия)
Тест А6 Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения. 1. Кристаллическая решетка хлорида кальция 1) ионная 2)молекулярная 3) металлическая 4) атомная 2. Молекулярное строение имеет 1) ртуть 2) бром 3) гидроксид натрия 4) сульфат калия 3. Атом является структурной частицей в кристаллической решетке 1) метана 2) водорода 3) кислорода 4) кремния 4. Вещества, обладающие твёрдостью, тугоплавкостью, хорошей растворимостью в воде, как правило, имеют кристаллическую решетку: 1) молекулярную 2) атомную 3) ионную 4) металлическую 5. Молекулярную кристаллическую решетку имеет 1) НВr 2) K2О 3) ВаО 4) КСl 6. Вещества с атомной кристаллической решеткой 1) очень твёрдые и тугоплавкие 2) хрупкие и легкоплавкие 3) проводят электрический ток в растворах 4) проводят электрический ток в расплавах. 7. Молекулярную кристаллическую решетку имеет 1) Са3Р2 2) СО2 3) SO2 4) АlF3 8. Ионную кристаллическую решетку имеет каждое из веществ, расположенных в ряду 1) натрий, хлорид натрия, гидрид натрия 2) кальций, оксид кальция, карбонат кальция 3) бромид натрия, сульфат калия, хлорид железа (II) 4) фосфат магния, хлорид калия, оксид фосфора (V) 9. Кристаллическая решетка графита 1) ионная 2) молекулярная 3) атомная 4) металлическая 10. Вещества, обладающие твердостью, тугоплавкостью, хорошей растворимостью в воде, как правило, имеют кристаллическую решетку 1) молекулярную 2) ионную 3) атомную 4) металлическую 11. Молекулярную кристаллическую решетку имеет 1) кремний 2) оксид углерода(IV) 3) диоксид кремния 4) нитрат аммония 12. Кристаллическая решетка галогенов 1) атомная 2) ионная 3) молекулярная 4) металлическая 13. К веществам с атомной кристаллической решеткой относятся 1) натрий, фтор, оксид серы (IV) 2) свинец, азотная кислота, оксид магния 3) бор, алмаз, карбид кремния 4) хлорид калия, белый фосфор, йод 14. Молекулярное строение имеет 1) цинк 2) нитрат бария 3) гидроксид калия 4) бромоводород 15. Вещества твердые, прочные, с высокой температурой плавления, расплавы которых проводят электрический ток, имеют кристаллическую решетку 1) металлическую 2) молекулярную 3) атомную 4) ионную 16. Ионы являются структурными частицами 1) кислорода 2) воды 3) оксида углерода (IV) 4) хлорида натрия 17. Немолекулярное строение имеют все неметаллы группы 1) углерод, бор, кремний 3) кислород, сера, азот 2) фтор, бром, иод 4) хлор, фосфор, селен 18. Кристаллическую структуру, подобную структуре алмаза, имеет 1) кремнезем 2) оксид натрия 3) оксид углерода (II) 4) белый фосфор Р4 19. Атом является структурной частицей в кристаллической решетке 1) метана 2) водорода 3) кислорода 4) кремния 20. Молекулярную кристаллическую решетку имеет каждое из двух веществ 1) графит и алмаз 2) кремний и йод 3) хлор и оксид углерода(IV) 4) хлорид бария и оксид бария 21. Атомную кристаллическую решетку имеет каждое из двух веществ 1) оксид кремния (IV) и оксид углерода (IV) 2) графит и кремний 3) хлорид калия и фторид натрия 4) хлор и йод 22. Молекулярное строение имеет 1) натрий 2) фруктоза 3) фосфат натрия 4) оксид натрия 23. Молекулярная кристаллическая решетка характерна для каждого из веществ, расположенных в ряду 1) хлорид калия, азот, метан 2) иод, диоксид углерода, озон 3) алюминий, бром, алмаз 4) водород, сульфат магния, оксид железа (III) 24. Оксид кремния тугоплавок, нерастворим в воде. Его кристаллическая решётка 1) атомная 2) молекулярная 3) ионная 4) металлическая 25. В зависимости от характера частиц, образующих кристалл, и от природы сил взаимодействия между ними различают четыре типа кристаллических решеток: 1) ионные, атомные, молекулярные и металлические 2) ионные, ковалентные, атомные и молекулярные 3) металлические, ковалентные, атомные и молекулярные 4) ионные, кубические, треугольные и слоистые 26. Кристаллическая решетка льда: 1) атомная 2) молекулярная 3) ионная 4) металлическая 27. Укажите вещество, которое в твердом состоянии имеет молекулярную кристаллическую решетку. 1) графит 2) натрий 3) гидроксид натрия 4) водород 28. Укажите вещество, которое в твердом состоянии имеет атомную кристаллическую решетку: 1) хлороводород 2) хлор 3) оксид кремния (IV) 4) оксид кальция 29. Для твердых веществ с металлической кристаллической решеткой характерна высокая. 1) растворимость в воде 2) электроотрицательность атомов 3) летучесть 4) электропроводность 30. Кристаллическое вещество образовано частицами Na+ и ОН-. К какому типу принадлежит кристаллическая решетка этого вещества? 1) атомная 2) молекулярная 3) ионная 4) металлическая 31. Немолекулярное строение имеет каждое из двух веществ: 1) S8 и O2 2) Fe и NaCl 3) CO и Mg 4) Na2CO3 и I2 32. Веществом молекулярного строения является 1) озон 2) оксид бария 3) графит 4) сульфид калия 33. Атомная кристаллическая решетка у простого вещества: 1) алмаз 2) медь 3) фтор 4) олово 34. Утверждение о том, что структурной частицей данного вещества является молекула, справедливо только для 1) алмаза 2) поваренной соли 3) кремния 4) азота 35. Ионную кристаллическую решетку имеет 1) вода 2) фторид натрия 3) серебро 4) бром 36. Простые вещества, имеющие одинаковый тип кристаллической решетки, образованы элементами 1) малых периодов 3) побочных подгрупп 2) главных подгрупп 4) больших периодов 37. Кристаллическую структуру, подобную структуре алмаза, имеет: 1) кремнезем SiO2 2) оксид натрия Na2O 3) оксид углерода(II) CO 4) белый фосфор Р4 38. Фосфин РН3 — это газ. Его кристаллическая решётка 1) атомная 2) молекулярная 3) ионная 4) металлическая 39. Из молекул состоят кристаллы. 1) сахара 2) соли 3) алмаза 4) серебра 40. Из разноимённо заряженных ионов состоят кристаллы 1) сахара 2) гидроксида натрия 3) алмаза 4) серебра 41. Какие частицы образуют кристалл нитрата натрия? 1) атомы Nа, N и О 3) ионы Nа+, NO3+ 5+ 22) ионы Nа, N ,О 4) молекулы NаNО3 42. Оцените правильность суждений о связи между строением и свойствами вещества. А. Среди веществ молекулярного строения есть газообразные, жидкие и твёрдые при обычных условиях. Б. Вещества с атомной кристаллической решеткой при обычных условиях твёрдые. 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны 43. Оцените правильность суждений о связи между строением и свойствами вещества: А. Если между частицами в кристалле прочная химическая связь, то вещество тугоплавко. Б. Все твёрдые вещества имеют немолекулярное строение 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны 44. Какие из приведенных утверждений верны: А. Вещества с молекулярной решеткой имеют низкие температуры плавления и низкую электропроводность. Б. Вещества с атомной решеткой пластичны и обладают высокой электропроводностью. 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны 45. Установите соответствие между веществом и типом его кристаллической решетки. ВЕЩЕСТВО ТИП КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ 1) поваренная соль А) молекулярная 2) серебро Б) ионная 3) углекислый газ В) атомная 4) графит Г) металлическая 5) глюкоза 46. Установите соответствие между типом кристаллической решетки и свойствами веществ. ТИП КРИСТАЛЛИЧЕСКОЙ СВОЙСТВА ВЕЩЕСТВ РЕШЕТКИ A) ионная 1) твердые, тугоплавкие, не растворяются в воде Б) металлическая 2) хрупкие, легкоплавкие, не проводят электрический ток В) атомная 3) пластичные, имеют различные температуры плавления, проводят электрический ток Г) молекулярная 4) твердые, тугоплавкие, хорошо растворяются в воде 47. Укажите ряд, характеризующийся уменьшением длины химической связи 1) SiCl4, MgCl2, AlCl3, NaCl 2) NaCl, MgCl2, SiCl4, AlCl3 3) NaCl, SiCl4, MgCl2, AlCl3 4) NaCl, MgCl2, AlCl3, SiCl4 48. Оцените правильность суждений о связи между строением и свойствами вещества. А. Если между частицами в кристалле прочная химическая связь, то вещество легко испаряется. Б. Все газы имеют молекулярное строение. 1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
Лекция 7
Зависимость свойств веществ от их
строения. Химическая связь. Основные
виды химической связи.
Рассматриваемые вопросы:
1. Уровни организации вещества. Иерархия структуры.
2. Вещества молекулярного и немолекулярного строения.
3.
4. Причины возникновения химической связи.
5. Ковалентная связь: механизмы образования, способы
перекрывания атомных орбиталей, полярность, дипольный момент
молекулы.
6. Ионная связь.
7. Сравнение ковалентной полярной и ионной связи.
8. Сравнение свойств веществ с ковалентными полярными и
ионными связями.
9. Металлическая связь.
10. Межмолекулярные взаимодействия.
Кристаллические решетки, видео
И в завершение подробное видео пояснения о свойствах кристаллических решеток.
Автор: Павел Чайка, главный редактор журнала Познавайка
При написании статьи старался сделать ее максимально интересной, полезной и качественной. Буду благодарен за любую обратную связь и конструктивную критику в виде комментариев к статье. Также Ваше пожелание/вопрос/предложение можете написать на мою почту [email protected] или в Фейсбук, с уважением автор.
Эта статья доступна на английском – Crystal Lattice in Chemistry.


